Modalità di valutazione della morfologia e della funzione ventricolare destra: modalità di esecuzione e scenari clinici
L’importanza della valutazione ventricolare destra in diversi scenari clinici, guida all’esecuzione di un esame completo per diagnosticare e monitorare diverse patologie
Introduzione
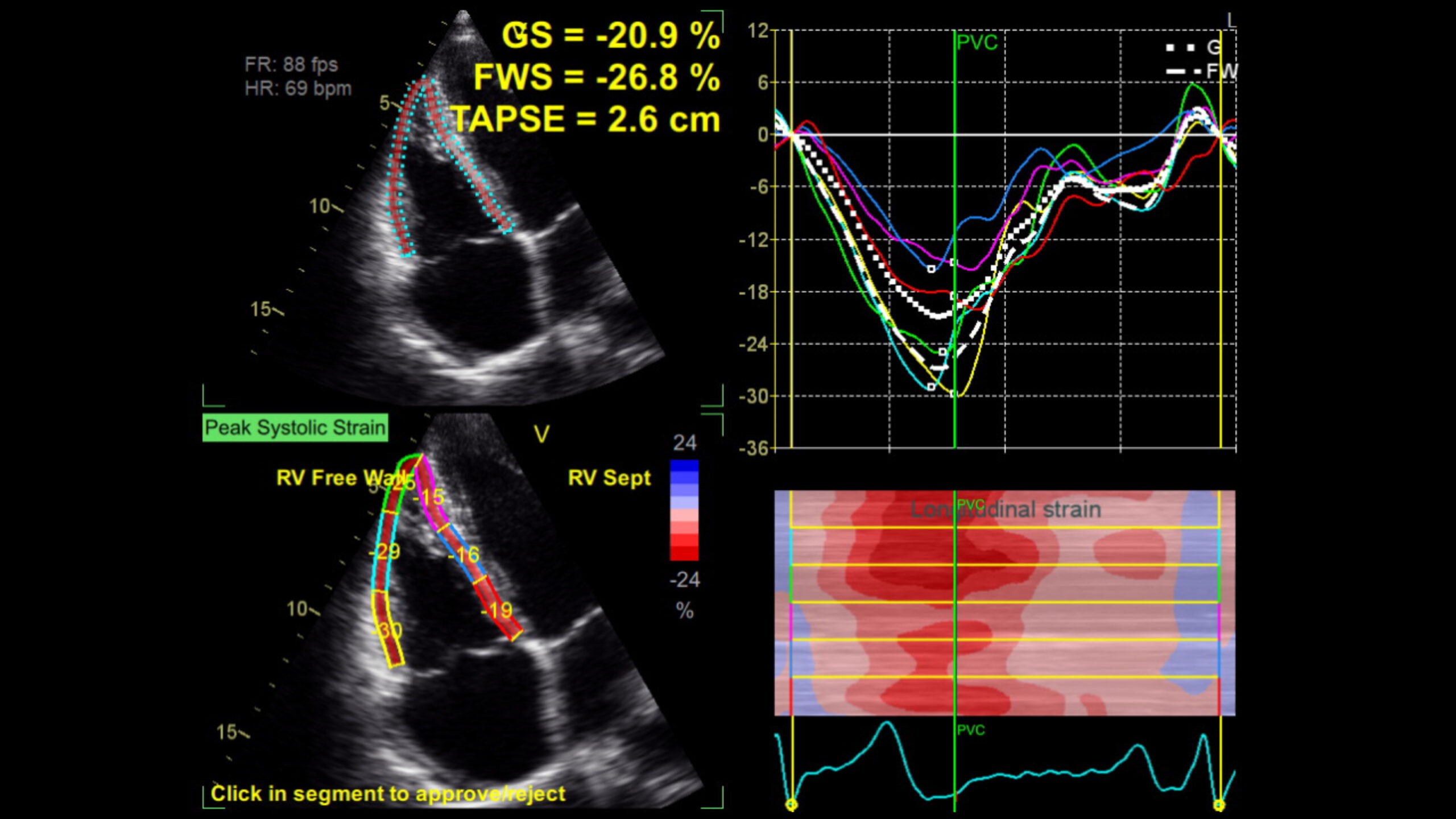
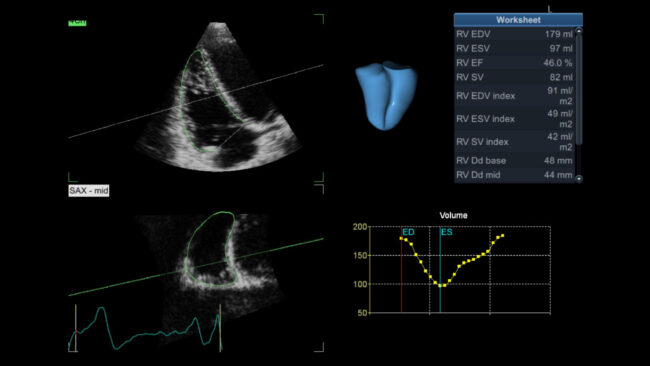
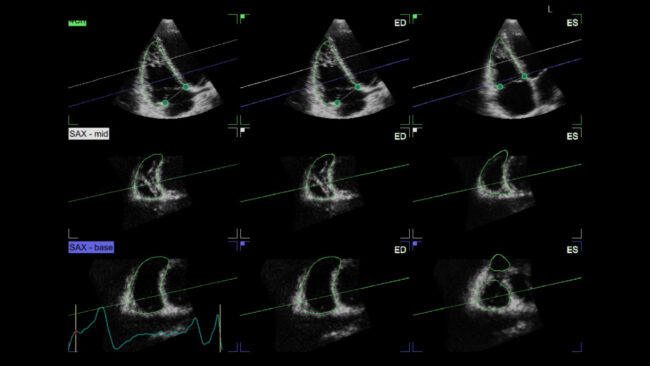
La valutazione del ventricolo destro (VD) mediante ecocardiografia bidimensionale (2D) si basa essenzialmente sui diametri basale, medio e longitudinale per la determinazione delle dimensioni, e sull’escursione sistolica longitudinale della tricuspide piano anulare (TAPSE), la velocità sistolica anulare tricuspide di picco (s’), la variazione di area frazionaria (FAC), lo strain della parete libera del VD (FWS) e l’ecografia tridimensionale (3D) per la definizione della funzione. In particolare, l’ecocardiografia 3D permette di superare i limiti derivanti dall’acquisizione del biplano (variabilità, accorciamento), di incorporare tutte le regioni del VD (apice, corpo, tratto di deflusso) e di valutare il loro contributo relativo all’espulsione del VD, di studiare l’anatomia mediante ricostruzioni 3D e misurare i volumi e la frazione di eiezione del VD, con accuratezza e riproducibilità simile a quella della risonanza magnetica cardiaca (RMC).
Ipertensione polmonare (IP)
L’IP è una condizione clinica caratterizzata dalla presenza di un aumento della pressione arteriosa polmonare media (> 25 mmHg a riposo misurata mediante cateterizzazione cardiaca destra). Può riconoscere molte cause diverse, per cui l’ecocardiografia gioca un ruolo chiave nell’algoritmo diagnostico e nella valutazione del suo impatto clinico-strumentale. La probabilità ecocardiografica di IP secondo le attuali Linee Guida si basa principalmente sulla presenza di un aumento della velocità di picco del rigurgito tricuspidale (> 2,8 m/s) e su altre variabili appartenenti a tre diverse categorie: dilatazione del VD (rapporto tra il diametro basale del VD e quello del ventricolo sinistro (VS) > 1,0), appiattimento del setto interventricolare per sovraccarico del VD (rappresentato da un indice di eccentricità del VS> 1,1), dilatazione o aumento della pressione arteriosa polmonare, dilatazione dell’inferiore vena cava (VCI) e dilatazione dell’atrio destro (AD). Altre caratteristiche ecocardiografiche tipiche della progressione di questa malattia sono l’ipertrofia e la disfunzione sistolica del VD, il rigurgito tricuspidale (IT) o polmonare e il versamento pericardico. La storia naturale di questa malattia prevede che all’inizio l’ipertrofia compensatoria del VD riesca a preservarne la funzione. Nel tempo, tuttavia, questo meccanismo adattivo si rompe e la disfunzione sistolica prende il sopravvento. In questi casi, la disfunzione sistolica deve essere indagata anche con tecniche avanzate come lo strain e l’ecocardiografia 3D, in quanto TAPSE è meno affidabile, poiché la contrazione del VD avviene principalmente sul piano trasverso e non sul piano longitudinale, come invece accade in condizioni fisiologiche.
Cardiopatie congenite
Le principali cardiopatie congenite dell’adulto caratterizzate da dilatazione del VD comprendono difetti del setto atriale (DIA), parziale ritorno anormale delle vene polmonari e, meno comunemente, anomalie della valvola tricuspide (malattia di Ebstein) e, estremamente raro, difetto congenito dello sviluppo della parete ventricolare destra (malattia di Uhl). Dal punto di vista fisiopatologico i DIA sono caratterizzati da un sovraccarico di volume a livello delle sezioni destre e da un overflow polmonare, che nel tempo determinano ad una progressiva dilatazione dell’AD e del VD e IP. Un DIA deve essere sempre sospettato quando c’è una dilatazione di AD e VD all’ecocardiogramma. Tra le caratteristiche tipiche di questa cardiopatia vi sono anche un aumento dell’indice di eccentricità del VS, un aumento del rapporto E/e’ a livello dell’annulus tricuspidale e una possibile ipertrofia del VD (in caso di malattia di lunga durata), mentre parametri come TAPSE e l’onda S’ possono essere paradossalmente aumentati, in quanto fortemente dipendenti dal carico volumetrico. L’ecocardiografia consente inoltre, mediante gli integrali velocità/tempo del Doppler pulsato e la misura dei diametri del tratto di efflusso del VD e del VS (da cui si ricava il rapporto Qp/Qs) di stimare l’entità del lo shunt tra le sezioni sinistra e destra. L’anomalia di Ebstein è caratterizzata da una morfologia anomala dei lembi tricuspidali, con lo spostamento dei lembi settali e posteriori verso l’apice del VD e un lembo anteriore ridondante. Questo spostamento verso il basso dell’anello funzionale provoca una parziale “atrializzazione” della parte pre-tricuspide del VD, che appare ipoplasica. Inoltre, lo spostamento della valvola tricuspide provoca una dissincronia della contrazione ventricolare destra e una riduzione della funzione sistolica. L’assenza di una valvola tra l’AD e la parte “atrializzata” del VD diminuisce l’uscita funzionale e contribuisce alla dilatazione delle due camere funzionali. L’entità dello spostamento della valvola varia considerevolmente, causando un’insufficienza tricuspidale da moderata a grave. Quando è presente una grave IT, la cianosi può svilupparsi anche a causa di uno shunt destro-sinistro attraverso un DIA o PFO, presente nell’80-90% dei pazienti. La gravità dell’IT e le dimensioni del VD “funzionale” sono i principali determinanti dei sintomi. Di conseguenza, la presentazione clinica può variare dall’assenza di sintomi alla cianosi e allo scompenso cardiaco. L’anomalia di Uhl è una condizione molto rara, caratterizzata dall’assenza parziale o totale dello strato miocardico del VD, con giustapposizione tra l’endocardio e l’epicardio. L’insufficienza cardiaca destra progressiva e la morte sono le manifestazioni più frequenti, mentre le aritmie ventricolari sono rare, probabilmente per l’assenza di un substrato miocardico. L’ecocardiografia è diagnostica, in quanto può mostrare la caratteristica severa dilatazione delle camere cardiache destre e l’assenza del miocardio ventricolare sinistro. Inoltre, può identificare aneurismi o trombi del VD e altre anomalie cardiache associate, come atresia polmonare e malformazioni della valvola tricuspide.
Infarto Ventricolo destro
L’infarto del ventricolo destro è molto meno frequente di quello del ventricolo sinistro perché lo spessore della parete è molto sottile con conseguente richiesta di ossigeno più bassa e la pressione intracavitaria è minore. Generalmente causato dall’ostruzione dell’arteria coronarica destra o di un’arteria circonflessa sinistra dominante, sta diventando comunque sempre più diagnosticato per l’evolversi delle metodologie di imagig. L’infarto miocardico destro può essere isolato o più frequentemente associato ad un infarto inferiore, aumentandone le complicanze (ipotensione e bradicardia) e la mortalità. Dal punto di vista ecocardiografico si nota riduzione della contrattilità spesso associato ad aumento del rigurgito tricuspidale e riduzione del preload ventricolare sinistro. Quando l’acinesia è presente solo a livello apicale bisogna ricordare nella diagnosi differenziale la S. di Takotsubo che può colpire anche isolatamente l’apice del ventricolo sinistro.
Cardiomiopatie
Sebbene la presenza di cardiomiopatia che coinvolge il VD di solito identifichi una specifica malattia cardiaca, inizialmente denominata “Cardiomiopatia ventricolare destra aritmogenica” e recentemente ribattezzata “Cardiomiopatia aritmogena” (ACM), è importante notare che varie cause possono coinvolgere VD e portare ad anomalie sia strutturali che funzionali. Il coinvolgimento del VD può essere presente in varie cardiomiopatie di origine sia genetica che non genetica, come la cardiomiopatia ipertrofica, la cardiomiopatia di Fabry, la cardiomiopatia dilatativa o la cardiomiopatia peripartum. Inoltre, il VD può essere affetto da malattie sistemiche con noto coinvolgimento cardiaco, come amiloidosi, sarcoidosi e sclerosi sistemica. Per quanto riguarda la ACM, nella sua descrizione originale era caratterizzato da un coinvolgimento esclusivo o almeno predominante del VD, più recentemente sono state scoperte le varianti biventricolare e dominante sinistra. È importante sottolineare che la fase presintomatica è preceduta da una fase preclinica, durante la quale si possono osservare alterazioni istologiche del miocardio, sebbene ancora clinicamente nascoste. L’identificazione della malattia nelle fasi iniziali può essere difficile, ma la diagnosi precoce è della massima importanza per prevenire la progressione della malattia e le manifestazioni aritmiche. Da questo punto di vista l’ecocardiografia gioca un ruolo fondamentale, dato che la Task Force Internazionale 2010 annovera tra i principali criteri per la diagnosi della ACM parametri ecocardiografici quali le anomalie della cinetica regionale del VD (acinesia, discinesia o aneurisma), oltre alle misurazioni quantitative del diametro del VD (considerando anomalo un diametro della RVOT ≥ 32 mm o 19 mm/ m2 nella finestra dell’asse lungo parasternale o ≥ 36 mm o 21 mm/m2 nell’asse corto parasternale finestra) e della variazione dell’accorciamento del VD (anormale se ≤ 33%). Il TAPSE invece è spesso inaffidabile nella valutazione della funzione di pompa del VD, dato che in ACM la disfunzione è correlata ad alterazioni della cinetica segmentaria. In linea di base, a differenza del fenotipo dominante destra, la sensibilità dell’ecocardiografia convenzionale per la diagnosi delle forme dominanti sinistra è inferiore. Tuttavia, le tecniche avanzate possono migliorare le prestazioni diagnostiche dell’ecocardiografia convenzionale, aiutando così a rilevare la malattia precoce e/o le varianti a predominanza sinistra. Inoltre, studi recenti hanno dimostrato che i risultati dell’ecocardiografia avanzata hanno un significato prognostico. Infatti, nell’ACM, l’analisi di deformazione mostra una ridotta deformazione longitudinale globale del VS e del VD, una ridotta deformazione longitudinale della parete libera e una maggiore dispersione meccanica del VD. Nello specifico, una deformazione longitudinale della parete libera con un valore maggiore di -23% e una dispersione meccanica del VD maggiore di 25-30 millisecondi riflettono una funzione sistolica ventricolare destra anormale.
Il cuore dell’atleta
Con il termine “cuore dell’atleta” si intende una serie di cambiamenti morfologici e funzionali risultanti dall’adattamento del miocardio ad un’attività fisica prolungata. Quando questo processo di rimodellamento è particolarmente pronunciato, può simulare una cardiopatia strutturale. L’attività sportiva aumenta il rischio di morte cardiaca improvvisa (SCD) e la causa più frequente di SCD nei giovani atleti (<35 anni) è la cardiopatia strutturale. Pertanto, lo scopo principale dello screening pre-partecipazione è la prevenzione della SCD negli atleti distinguendo tra cambiamenti fisiologici dovuti all’intensa attività fisica nel cuore dell’atleta e gravi malattie cardiache con caratteristiche morfologiche simili. Quando le caratteristiche cliniche ed elettrocardiografiche sembrano non essere correlate all’allenamento e sono sospette per una patologia, l’ecocardiografia rappresenta la metodica diagnostica di secondo livello. Dal punto di vista ecocardiografico, il cuore dell’atleta mostra un ispessimento della parete del VS armonico e simmetrico, con uno spessore settale massimo generalmente <12 mm e una funzione diastolica del VS sopra-normale (E/A> 2). Il VS è dilatato, con diametro telediastolico generalmente non superiore a 60 mm. Questi reperti ecocardiografici consentono la diagnosi differenziale rispettivamente con cardiomiopatia ipertrofica e cardiomiopatia dilatativa. Il processo di rimodellamento coinvolge anche il VD, che risponde all’aumento della gittata cardiaca con un aumento delle dimensioni e della massa. Il tipo di sport (gli sport combinati e di resistenza inducono cambiamenti più pronunciati), l’età e gli anni di allenamento sono predittori dell’allargamento del VS. Nonostante il significativo aumento delle dimensioni del VS, gli atleti di solito mostrano una normale funzione sistolica del VD. Da notare che la disfunzione sistolica VD acuta e transitoria è stata descritta dopo un intenso esercizio di resistenza. L’ecocardiografia standard è lo strumento di imaging iniziale. I valori normali dello spessore della parete ventricolare sono <0,5 cm, misurati nella finestra dell’asse lungo sottocostale o parasternale utilizzando l’imaging della telediastole in modalità M o 2D a livello del cordone ombelicale della valvola tricuspide. La dimensione del VD deve essere misurata utilizzando almeno il diametro basale del VD e il diametro longitudinale (tra la base del ventricolo destro e l’apice) nella finestra apicale a quattro camere. Inoltre, il rimodellamento ventricolare nel cuore dell’atleta è accompagnato da adattamenti extracardiaci, come la dilatazione della vena cava inferiore (valore medio = 26 mm, limite superiore = 40 mm, misurato dalla finestra sottocostale). Nuove tecniche ecocardiografiche possono essere utili per differenziare tra il cuore dell’atleta e la cardiopatia strutturale allo stadio iniziale. In generale, lo sforzo di tutte le camere cardiache è preservato nel cuore dell’atleta, a differenza di quanto accade nelle cardiomiopatie. La deformazione longitudinale globale del ventricolo sinistro (GLS) è solitamente normale nel cuore dell’atleta e non differisce con i controlli sani; pertanto, la sua riduzione dovrebbe far sorgere il sospetto di una malattia strutturale, soprattutto nel caso in cui siano presenti altri riscontri dubbi (clinici e/o strumentali). Un piccolo aumento del GLS durante l’ecocardiografia da stress può rappresentare un altro segno di malattia miocardica sottostante. Lo strain VD, data la sua capacità di identificare le anomalie del movimento della parete regionale, può essere utile per distinguere tra il cuore dell’atleta e l’ACM. Inoltre, sebbene gli atri possano essere dilatati sia nel cuore dell’atleta che nella cardiomiopatia, lo sforzo è ridotto solo in quest’ultima. Infine, l’ecocardiografia 3D rappresenta un valore aggiunto per la sua capacità di definire con precisione i volumi e la funzione biventricolare.
Conclusioni
Il VD è alterato in una moltitudine di stati patologici e parafisiologici. L’ecocardiografia rappresenta il primo strumento di indagine morfofunzionale, con l’attuale possibilità di utilizzare metodiche più avanzate come l’ecocardiografia con contrasto, deformazione e 3D. L’importanza della valutazione ecocardiografica del VD non si limita solo alla diagnosi di queste condizioni, ma ha un impatto terapeutico e prognostico significativo.