Nei nostri ambulatori ecocardiografici sono sicuramente ora più utilizzati la velocità tricuspidalica come “cut-off” diagnostico ed il parametro “TAPSE/PAPs” (anche se in misura minore) L’uso di una terapia duplice di associazione precoce è diventato routinario in molti pazienti
Aspetti positivi e negativi delle recenti linee guida vengono quotidianamente affrontati negli ambulatori per l’ipertensione polmonare delle nostre cardiologie, ed ancora molti rimangono gli aspetti irrisolti, in primis le armi terapeutiche che impattino sulla mortalità
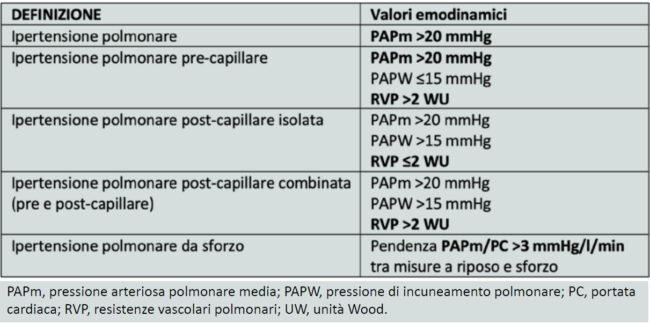
È passato un anno da quando sono state pubblicate al Congresso Europeo di Barcellona le linee guida congiunte della società europea di cardiologia (ESC) e pneumologia (ERS) sulla ipertensione polmonare (IP), a distanza di ben 7 anni dalle precedenti. Le novità hanno riguardato diversi aspetti, tra i quali la classificazione, la diagnosi, la stratificazione del rischio e le indicazioni terapeutiche in base all’eziologia ed alla presenza di comorbidità. Ma quali aspetti sono stati realmente adottati dai nostri ambulatori per l’ipertensione polmonare e quali rimangono meno praticabili? La prima importante novità delle linee guida 2022 consiste nell’aver modificato i criteri emodinamici per la diagnosi di ipertensione polmonare (IP) (Figura 1): il valore di pressione arteriosa polmonare media (PAPm) è stato ridotto da 25 mmHg a 20 mmHg.
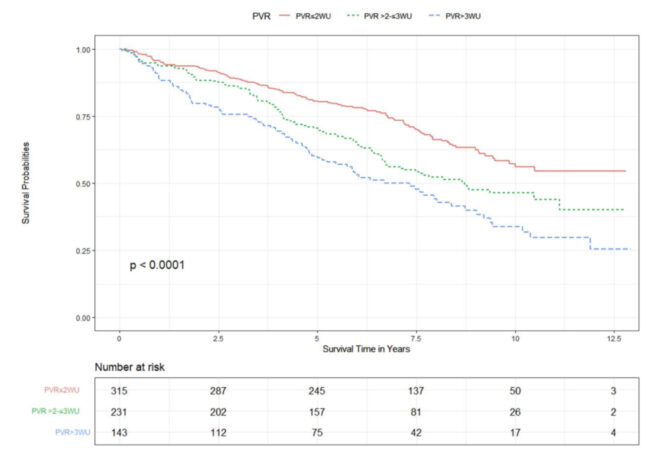
Tale valore è suffragato da studi che hanno valutato il limite superiore del range di normalità della PAP in soggetti sani e la rilevanza prognostica di un’elevata PAP. Similmente, il cut-off diagnostico del valore di resistenze vascolari polmonari (RVP) è sceso da 3 a 2 unità Wood (UW). Tale modifica è frutto degli studi eseguiti su sottogruppi di pazienti del gruppo 1 nei quali è stato visto come un lieve incremento delle RVP possa avere un significato prognostico negativo. È stata, inoltre, reintrodotta la definizione di IP da sforzo basata su una differenza nella pendenza tra PAPm e portata cardiaca (PC) (PAPm/PC slope) >3 mmHg/l/min in condizioni di riposo e durante esercizio fisico. L’impatto di queste modifiche sulla sensibilità diagnostica in Italia può essere valutato centro per centro, ma per l’assenza di un registro nazionale (oltre che regionale) non è oggettivabile. Recentemente, invece, sono stati pubblicati dei dati dal registro EVIDENCE-PAH UK che ha raccolto i dati dei pazienti sottoposti a cateterismo cardiaco destro dal 2009 al 2017 nei 7 centri UK che si occupano di ipertensione arteriosa polmonare (IAP). Dei 2929 cateterismi, il 43% aveva una PAPm tra 21 e 24 che dimostra un notevole impatto sulle nuove diagnosi. Inoltre, la presenza di PVR tra 2 e 3 definiva un gruppo con mortalità statisticamente inferiore al gruppo con PVR >3 (Figura 2).
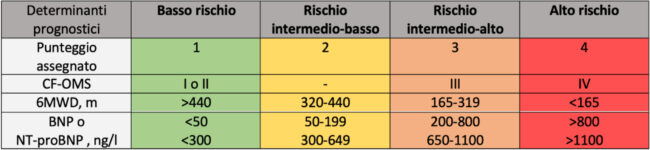
Va comunque sottolineato come tale aggiornamento della classificazione purtroppo non si accompagna (al momento) ad un aumento dei pazienti trattabili con terapia specifica: tutti gli studi registrativi dei farmaci specifici hanno utilizzato per la diagnosi i vecchi cut-off di PAPm e RVP. Nelle ultime linee guida viene raccomandato, per il sospetto diagnostico all’ecocardiogramma, l’utilizzo della velocità di picco tricuspidalica al posto delle famose “PAPS” che effettivamente con fatica inizia a intravedersi sulle risposte dei nostri ambulatori ecocardiografici, mentre ancora è poco diffuso il parametro “TAPSE/PAPs”. Nelle realtà cardiologiche italiane, per quanto raccomandato dalle linee guida, è ancora poco attuato il concetto di “fast-track”, ovvero di centralizzazione sollecita al centro esperto/ad alto volume dei pazienti con caratteristiche di alto rischio: il primo contatto del paziente avviene spesso in centri non ad alto volume, che possono però (senza ritardare l’inizio della terapia) eseguire i primi esami ad inquadramento almeno della tipologia di IP. La stratificazione del rischio alla diagnosi è stata differenziata per pazienti incidenti e prevalenti, ma sono state mantenute le 3 classi di rischio per le nuove diagnosi (bassointermedio- alto), modificando i limiti di mortalità. È stato aggiunto il test cardiopolmonare tra le indagini funzionali e la risonanza magnetica cardiaca (RMN) tra i criteri diagnostici dando a questa ultima un ulteriore risalto inserendo anche nuovi parametri di riferimento. Sono stati rivalutati i criteri dei parametri già esistenti, modificando il cutoff dell’NT proBNP (<300 pg/ml per il basso rischio, >1100 per il rischio alto) ed introducendo tra i criteri ecocardiografici la valutazione dell’accoppiamento ventricolo arterioso (TAPSE/sPAP >0.32 mm/ mmHg per il rischio basso; < 0.19 mm/mmHg per il rischio alto). Tale parametro, facilmente eseguibile durante l’esame ecocardiografico, era stato già introdotto nelle linee guida dell’embolia polmonare ma bisogna avere la certezza della corretta misurazione della pressione atriale destra indiretta dai valori della vena cava inferiore. È stato, inoltre, introdotto il parametro di saturazione venosa mista (SVO2) al cateterismo cardiaco destro (SvO2 >65% per i pazienti a rischio basso, SvO2 <60% per il rischio alto) visto il suo alto potere predittivo prognostico. La rivalutazione del paziente viene raccomandata a 3-6 mesi dalla diagnosi e la stratificazione del rischio proposta è differente permettendo di categorizzare il paziente in: rischio basso, intermedio-basso o intermedioalto ed alto rischio. La nuova stratificazione si basa solo su criteri clinico-funzionali (classe funzionale e 6 walking test) e laboratoristici (peptidi natriuretrici atriali). Non compaiono quindi criteri o strumentali (ecocardiogramma, RMN, cateterismo destro) per la stratificazione del rischio nel followup (Figura 3) anche se vengono “fortemente raccomandati”: la sensazione ad un anno dalle linee guida è che il clinico non ne riesca a fare a meno, in particolare per l’ecocardiogramma, anche perché alcuni parametri (distanza percorsa in 6’ e classe funzionale) possono essere falsate da età e capacità fisica.
6MWD, distanza percorsa al test del cammino di 6 min; BNP, pepSde natriureSco di Spo B; CF-OMS, classe funzionale dell’Organizzazione Mondiale della Sanità; BNP, propepSde natriureSco di Spo B ; NT-proBNP, frammento N-terminale del propepSde natriureSco di Spo B.
Figura 3 – Variabili utilizzate nel modello semplificato per la valutazione del rischio nel follow-up basato su quattro categorie
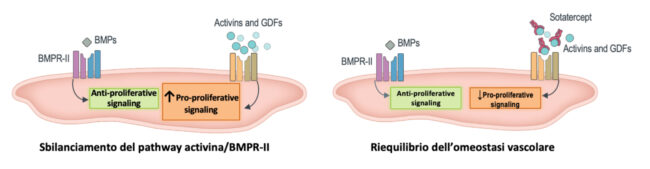
L’età avanzata e la crescente presenza di comorbidità cardiovascolari (obesità, ipertensione, fibrillazione atriale, disfunzione diastolica) e polmonari (pneumopatia lieve, ridotta diffusione polmonare del monossido di carbonio o DLCO) sono state finalmente introdotte nelle nuove linee guida con l’etichetta di IAP “atipica” nel nuovo algoritmo di trattamento: in tali pazienti è consigliata una terapia singola orale per la scarsa risposta ai farmaci specifici, e questo dà maggiore tranquillità ai clinici che si trovano a gestire sempre di più tali pazienti. Le nuove linee guida nei pazienti invece con IAP “tipica” confortano il clinico nell’“aggredire” la patologia con due farmaci (inibitore recettore endotelina ed inibitore delle fosfodiesterasi) o tre (con prostanoide endovena o sottocute) già alla diagnosi in base alla stratificazione del rischio, anche se non chiariscono modalità e tipologia di associazione soprattutto nei primi 1-2 mesi. Non vi è, sostanzialmente, più spazio per la monoterapia se non per alcuni specifici sottogruppi (vasoreattività confermata, ipertensione cronica tromboembolica trattata chirurgicamente e non). A 3-6 mesi della diagnosi, in caso di rischio intermedio-basso viene preso in considerazione l’utilizzo della triplice terapia orale (con selexipag, agonista del recettore delle prostacicline) e/o lo shift da inibitore della fosfodiesterasi 5 (PD5i) a stimolatori della guanilato ciclasi solubile (SGc, riociguat). Nella flow chart terapeutica non è stata inserita una nuova linea di farmaci che agisce su una via differente da quelle sin ora conosciute: sotatercept, farmaco biologico a somministrazione sottocutanea che mira ad inibire il segnale cellulare associato all’ iperproliferazione vascolare ed al rimodellamento patologico dei vasi polmonari, ristabilendo l’equilibrio funzionale dei fattori di crescita (figura 4).
Lo spostamento del segnale pro-proliferaSvo aumenta il rischio di ipertensione arteriosa e contribuisce alla patogenesi della mala\a modulando la sopravvivenza cellulare e la proliferazione vascolare. Sotatercept, cosStuito da una proteina di fusione ricombinante, agisce come trappola del ligando ed elimina l’eccesso di acSvina A e altri ligandi inibendo il segnale di quesS. Di conseguenza, si riSene che sotatercept riequilibri il segnale pro-proliferaSvo e anSproliferaSvo modulando la proliferazione vascolare.
Figura 4 – Meccanismo d’azione di sotatercept
Nello studio STELLAR, esso ha mostrato effetti positivi sulla distanza percorsa al test del cammino, e su alcuni endpoint secondari tra cui il tempo al peggioramento clinico, nei pazienti con IAP già in terapia specifica. In conclusione ad un anno, dalla pubblicazione delle linee guida ESC/ERS sulla PH vi sono aspetti recepiti ed altri ancora non entrati nella pratica clinica, ma abbiamo finalmente un nuovo farmaco che apre una “quarta” via terapeutica per la IAP, per cui ci si auspica di avere ulteriori dati a supporto che permettano un update della flowchart terapeutica.