La traiettoria di sviluppo di un individuo si definisce attraverso una rete complessa di interazioni tra geni (nature) e fattori ambientali (nurture)
La teoria della riprogrammazione fetale e le malattie cardiovascolari Il ruolo dell’epigenetica nello sviluppo delle NCDs
Nonostante i notevoli progressi nel campo della prevenzione, della diagnostica e del trattamento, l’incidenza delle non-communicable diseases (NCDs), come diabete, patologie cardiovascolari, malattie respiratorie croniche ed oncologiche, è in aumento in tutto il mondo.
È noto ormai da tempo che il benessere di un individuo nell’arco della vita è strettamente influenzato dalle interazioni tra il suo background genetico, l’ambiente, ed il suo stile di vita. Studi sperimentali su modelli animali e osservazioni epidemiologiche hanno portato alla luce il ruolo dei fattori ambientali che agiscono nelle fasi precoci dello sviluppo nell’influenzare il rischio individuale di sviluppare patologie croniche non trasmissibili(1).
Infatti, nei momenti di massima plasticità dell’organismo, come durante lo sviluppo prenatale e il primo periodo postnatale, le influenze dell’ambiente sui processi plastici fisiologici possono porre le basi “pato-fisiologiche” del rischio di malattia, con potenziali effetti avversi per l’individuo in momenti successivi della vita.
Tra gli anni ’80 e ’90 l’epidemiologo britannico David Barker, studiando la correlazione tra basso peso alla nascita ed aumentato rischio di malattia cardiovascolare nell’età adulta, introdusse per la prima volta il concetto di “fetal programming” (programmazione fetale), definendolo come risposta adattativa del feto, messa in atto quando l’ambiente ottimale in cui questo cresce e si sviluppa viene perturbato da fattori avversi.
Gli studi epidemiologici di David Barker hanno posto le basi della teoria del programming fetale, secondo cui patologie dell’età adulta hanno origine da cambiamenti morfo-funzionali e metabolici che insorgono in periodi critici dello sviluppo.
Barker e colleghi ipotizzarono che mediante il “programming” il feto è in grado in condizioni sfavorevoli di mettere in atto una risposta adattativa sviluppando un fenotipo definito “parsimonioso”(2). La madre trasmette al feto informazioni che gli forniscono una previsione dell’ambiente in cui nascerà. Per esempio, se la nutrizione materna è povera e inadeguata, il metabolismo del nascituro si adatta e si prepara per sopravvivere in condizioni di scarsità di nutrienti.
Però tale adattamento diventa svantaggioso nel momento in cui la previsione fornita dalla madre risulta diversa dalla situazione in cui il bambino si troverà a vivere. Un ambiente postnatale caratterizzato da abbondanza di cibo porterà, dunque, l’individuo dal fenotipo frugale verso il rischio di obesità e patologie metaboliche.
L’incidenza delle non-communicable diseases (NCDs), come diabete, patologie cardiovascolari, malattie respiratorie croniche ed oncologiche, è in aumento in tutto il mondo.
È su quella che viene definita la “Barker theory” che si basa la scienza delle Origini dello Sviluppo della Salute e della Malattia (DOHaD)(3). Secondo il modello DOHaD, il rischio di sviluppare NCDs dipende dai fattori ambientali che agiscono nelle primissime fasi di vita e non soltanto dalla genetica o dallo stile di vita in età adulta. Tale modello trae origine dalla convergenza degli sforzi della ricerca in campi diversi (studi epidemiologici retrospettivi sulle popolazioni umane, biologia evolutiva e dello sviluppo, antropologia, medicina, genetica, studi sulla nutrizione e studi sulla fisiologia animale e umana). Numerose evidenze scientifiche, ottenute negli ultimi anni, indicano che i processi epigenetici siano tra i meccanismi principalmente coinvolti nel fetal programming. La traiettoria di sviluppo di un individuo si definisce attraverso una rete complessa di interazioni tra geni (nature) e fattori ambientali (nurture), in cui i meccanismi epigenetici fungono da collegamento, controllando quando e come geni distinti devono attivarsi.
L’epigenoma “programma” il genoma, determinando l’espressione di specifici geni in momenti ben determinati della vita di un organismo. I meccanismi epigenetici sono in grado di influenzare la regolazione dell’espressione genica con diverse modalità, ma tre sono quelle più note attraverso le quali essi agiscono: la metilazione del DNA, la modifica degli istoni e l’attività degli RNA non codificanti, in particolar modo dei miRNA(4).
L’assetto epigenetico nelle cellule di un individuo viene stabilito in due momenti critici del suo sviluppo che si svolgono nella vita intrauterina: il pre-impianto dell’embrione e lo sviluppo delle cellule germinali primordiali nel feto. Le specifiche modificazioni epigenetiche stabilite in quei momenti vengono trasmesse in modo relativamente stabile nei processi di proliferazione cellulare. I meccanismi epigenetici sono però processi dinamici, difatti modificazioni epigenetiche possono verificarsi durante tutto l’arco della vita stessa, ma i cambiamenti epigenetici indotti durante lo sviluppo embrionale sembrano avere un impatto molto maggiore sull’organismo; le alterazioni che si verificano nelle cellule staminali embrionali singole possono essere trasmesse nelle divisioni mitotiche consecutive interessando molte più cellule (e di conseguenza i tessuti e gli organi che da queste origineranno), rispetto alle alterazioni che si verificano in cellule staminali adulte e/o somatiche durante lo sviluppo postnatale.
Evidenze scientifiche dimostrano che le modificazioni epigenetiche acquisite possono essere trasmesse alle generazioni successive, pertanto si potranno avere effetti inter- e trans-generazionali, anche se i cambiamenti nell’espressione genica non alterano però la sequenza del DNA. I dati più numerosi della letteratura a supporto della DOHaD provengono da studi sulle malattie metaboliche e cardiovascolari. Sempre più numerose sono le osservazioni epidemiologiche di come fattori perinatali possano determinare l’insorgenza di obesità e quadri dismetabolici nella vita adulta. Un fattore importante è rappresentato dal BMI della madre pre-gravidanza; figli di donne con BMI > 25 hanno un rischio di diventare obesi rispettivamente di 1.7 durante l’infanzia e di due volte in età adulta. Durante la gravidanza, invece, l’eccessivo incremento ponderale della madre, una dieta ricca di grassi, una scarsa attività fisica e soprattutto la comparsa di diabete gestazionale, correlano con la comparsa di obesità e diabete in età adulta, come anche il basso peso del nascituro. Esistono dati che la preeclampsia, l’uso di sostanze voluttuarie, come fumo e alcol, l’uso di alcuni farmaci durante la gravidanza correlano con un maggior rischio di sviluppare malattie cardiovascolari (CVD) in età adulta (5). Interessanti sono le osservazioni derivanti prevalentemente da modelli animali, come alcuni fattori riguardanti la dieta, l’inquinamento ambientale, condizioni di stress possano avere un effetto sui gameti sia maschili che femminili, quindi anche la fase pre-concepimento potrebbe avere un ruolo nella suscettibilità del nascituro a sviluppare CVD nell’età adulta. Tale predisposizione perinatale ovviamente diventa ancora più manifesta se non vi è aderenza da parte del singolo individuo adulto al rispetto di adeguati stili di vita.
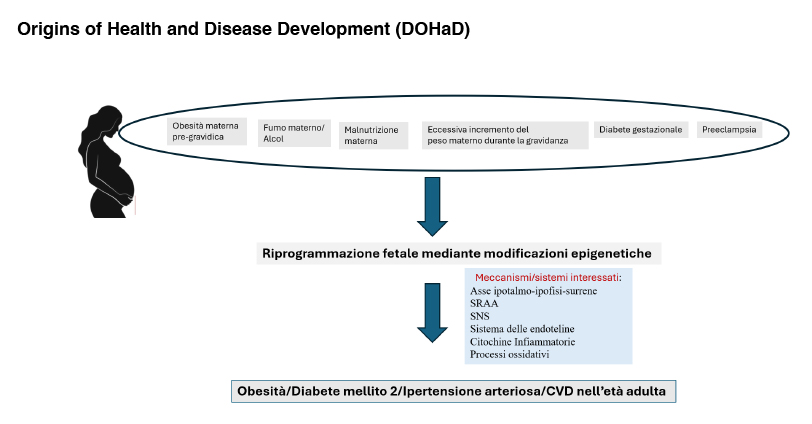
I meccanismi implicati nell’insorgenza delle malattie cardiovascolari legate al fenomeno della riprogrammazione fetale non sono ancora ben noti. Sembrerebbero avere un ruolo variazioni a carico dell’asse ipotalamo-ipofisi-surrene, del sistema renina-angiotensina-aldosterone, del sistema nervoso simpatico; un ruolo viene anche attribuito al sistema delle endoteline, alla produzione di citochine infiammatorie e all’attivazione dei processi ossidativi (Figura 1). Le informazioni provenienti dagli studi sulla DOHaD ci suggeriscono che oggi l’approccio alla prevenzione delle malattie cardiovascolari non può prescindere dal mettere in atto strategie di “prevenzione primordiale”, mirate a ridurre il rischio delle NCDs agendo già in quella finestra temporale che si estende dal concepimento fino ai primi anni di vita.
Diventa fondamentale la collaborazione tra diverse discipline scientifiche per ampliare le nostre conoscenze, ma anche e soprattutto rendere edotti e consapevoli i futuri genitori che la responsabilità della salute dei loro figli inizia già ancor prima del concepimento. ♥
L’approccio alla prevenzione delle malattie cardiovascolari non può prescindere dal mettere in atto strategie di “prevenzione primordiale”, mirate a ridurre il rischio delle NCDs.
Bibliografia
- Budreviciute A, et al. Management and Prevention Strategies for Non-communicable Diseases (NCDs) and Their Risk Factors. Front Public Health. 2020 Nov 26; 8:574111.
- Barker DJ. The fetal and infant origins of adult disease. BMJ. 1990; 301:1111.
- Barker DJ. The origins of the developmental origins theory. J Intern Med. 2007 May; 261(5):412-.
- Ryznar JR, Phibbs L, Van Winkle LJ. Epigenetic modification at the center of the Barker hypothesis and their transgenerational implications. Int J Environ Res Public Health. 2021; 18:12728.